Parkinson’s disease (PD) is a slowly progressive neurodegenerative disease clinically characterized by progressive motor impairment in affected people. Synaptic and axonal degeneration is followed by loss of dopaminergic neurons in the substantia nigra leads to reduced levels of dopamine in the nigrostriatal circuitry. Besides dopaminergic cell loss, intracellular formation of Lewy bodies, consisting predominantly of aggregated alpha-synuclein, has been suggested to be crucial in the pathogenesis of this disease.
PD is a complex, multifactorial disease in which different factors concur to the pathogenic process. In vitro models (established cell lines, primary cell cultures or lesion models) offer the advantage of a controlled environment favorable for exploring single pathogenic mechanisms and the genes/proteins involved.
On the cellular level, research in PD focuses on:
- Neurotoxicity (MPP+, 6-OHDA, BSO,…)
- Excitotoxicity (NMDA, glutamate,…)
- Mitochondrial dysfunction
- Defects in protein degradation
QPS Austria offers several cellular solutions to model PD pathology in vitro:
The degeneration of midbrain dopaminergic neurons is the hallmark of the pathology of Parkinsons Disease (PD). Dopaminergic neurons represent less than 1% of the total number of neurons in the brain, though regulating such important brain functions as motor control, motivation, and working memory. Primary cultures constitute one of the most relevant models to investigate properties and characteristics of dopaminergic neurons.
QPS Austria provides primary dopaminergic TH (tyrosine hydroxylase) positive neurons from the ventral mesencephalon of rats. These cultures can be submitted to various stress agents that mimic PD pathology (MPP+, 6-OHDA) and to neuroprotective compounds in order to stop or slow down neuronal degeneration. A software supported automatic quantification method allows the determination of the following end points such as TH cell numbers, neurite outgrowth or apoptosis. A controlled regeneration or the prevention of degeneration of dopaminergic neurons are promising therapeutic approaches.
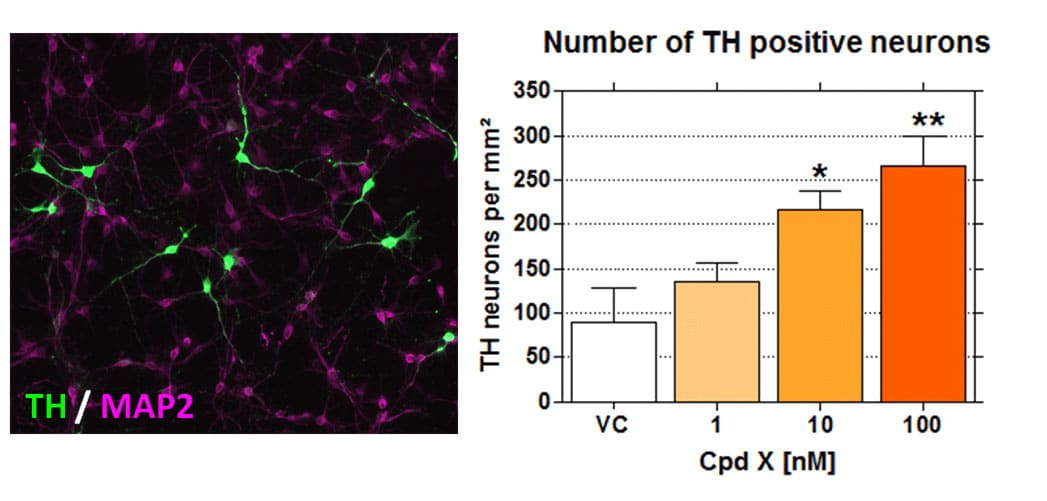
Figure: Effects of a developmental Compound X on the number of primary rat TH neurons from the ventral mesencephalon.
PD involves the degeneration of nigrostriatal dopaminergic (DA) neurons. This pathology can be modeled in experimental animals by the administration of MPTP (1-metyl-4-phenyl-1, 2, 3, 6-tetrahydropyridine), a neurotoxin which is converted in the brain into MPP+ (1-methyl-4-phenylpyridinium) by the enzyme MAO-B a toxin which selectively destroys DA neurons and causes anatomical, behavioral, and biochemical changes similar to those seen in Parkinson’s disease.
In vitro Parkinsonism can be modeled by the administration of MPP+ to different cell culture systems. QPS Austria provides several cell culture models for MPP+ induced Parkinsonism, as primary cortical neurons (Figure), primary rat TH neurons, SH-SY5Y and many more.
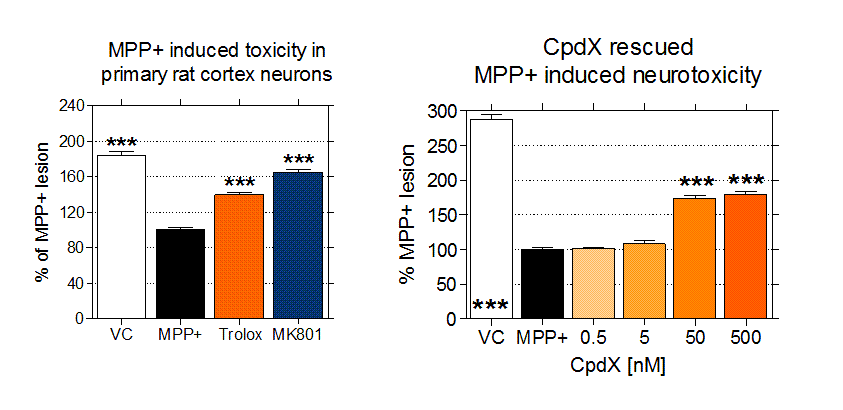
Figure: Effects of known compounds as Trolox and MK-801 (left) and Compound X (right) on MPP+ induced toxicity in primary rat cortex neurons.
Primary fibroblasts available from patients clinically affected by:
- Parkinson Disease (PD)
- Leber’s Hereditary Optic Neuropathy (LHON)
- Friedreich Ataxia (FRDA)
Skin fibroblasts present a system with defined mutations and the cumulative cellular damage of the patients and can thus serve as additional model to other cell systems as primary neurons or neuroblastoma cell lines.
To mimic disease related lesions of Parkinson‘s Disease, BSO (DL-buthionine-SR-sulfoximine) is applied for 48h to induce a toxic insult in PD cells. Cells are treated with or without Idebenone and cell viability is determined by MTT assay. Other possible toxic insults are available as MPP+, H2O2, Abeta1-42, 6-OHDA. Evaluation assays may range from cell viability to apoptosis assays or Mitochondrial related assays (activity, distribution, shape, membrane depolarization,…).
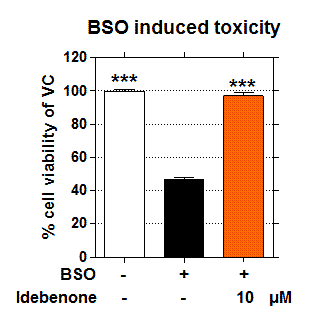
Figure: Effects of Idebenone on BSO induced neurotoxicity in human PD Fibroblasts.
